소프트웨어, 무형자산을 보유한 기업 위주의 포트폴리오 보완을 위해 유형의 사업을 원활히 확장하고 있는 기업을 찾아보게 되었다.
물론 향후 성장에 대한 근거가 충분하여 매수할 때 다소 비싼 밸류에이션으로 실수를 했더라도 성장이 실수를 보완해주어야 하는 기업이라는 대전제는 충족하는 기업중에 열심히 찾아봤다.
많은 인터넷 상의 소비자 행동이 자동화/합리화되어가고 있는 가운데,
일상적인 소비는 여전히 취향과 습관의 영역으로 개별 기업이 거대 시스템으로부터 독립적으로 해자를 구축하기 용이한 분야라 할 수 있다.
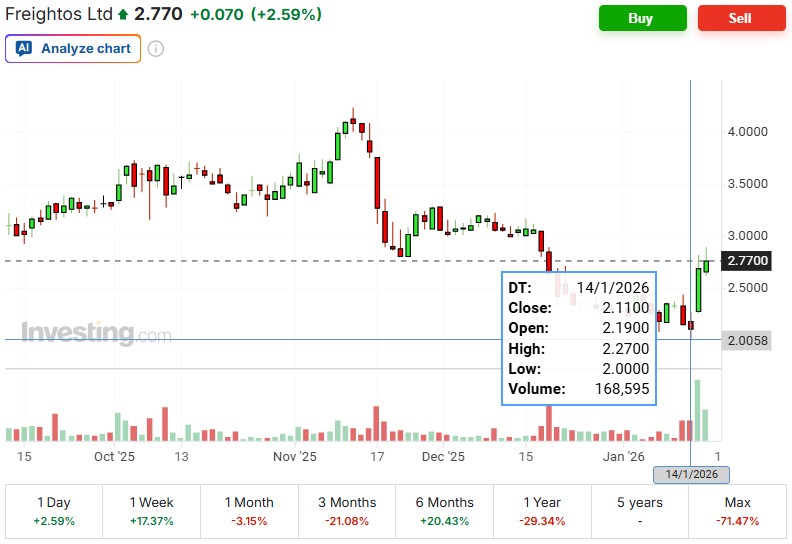
필터링을 통해 이 분야에서 빠르게 성장하고 있고, 앞으로도 그럴 수 있는 Dutch Bros(NYSE : BROS)를 발굴해봤다.
아래 영상을 보면 BROS 브랜드의 특징을 좀 더 쉽게 이해할 수 있을 거 같다.
BROS의 성장성
매출의 구분 및 매출 추이
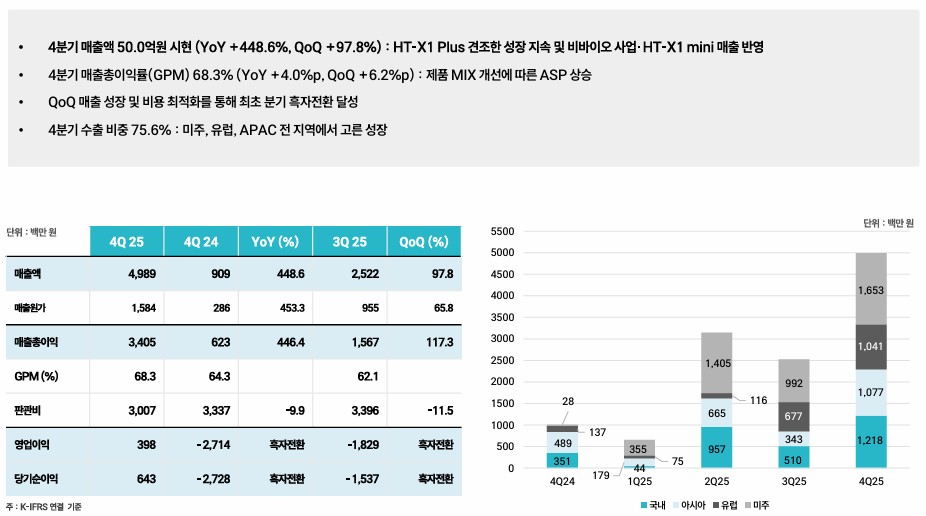
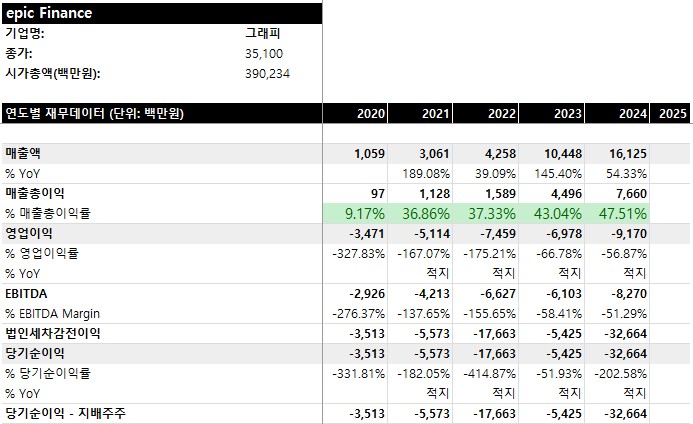
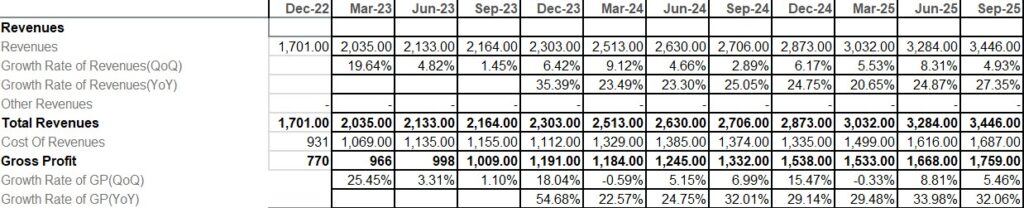
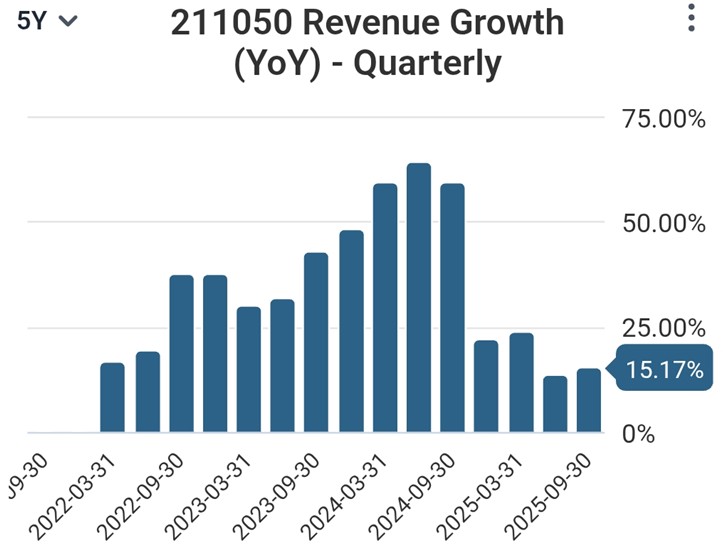
BROS는 다소 감속되기도 했지만, 아래 표에서 볼 수 있듯이 상당한 규모 확장에도 불구하고 30%에 가까운 충분히 높은 수준의 성장률을 최근 3년 동안 유지하여 매출이 두 배 증가하였다.
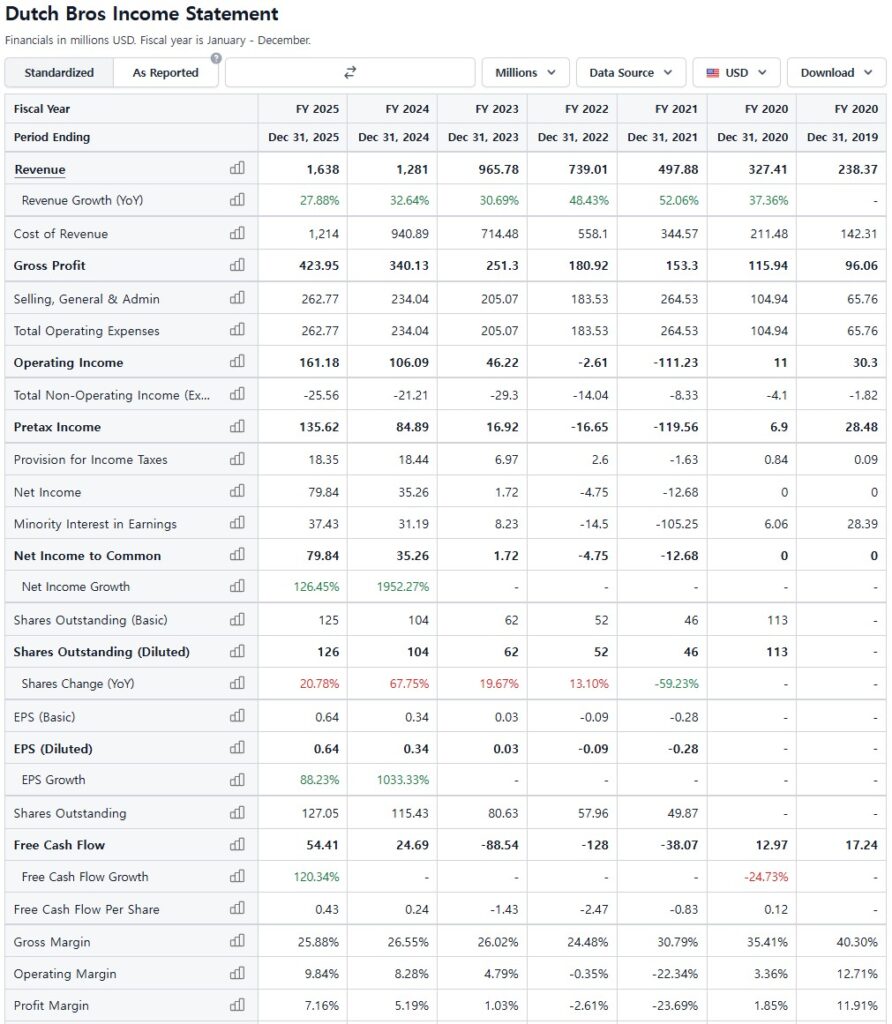
Dutch Bros는 음료 체인의 성격상 매장 운영 수익이 핵심이다.
SEC filing은 매출을 두 부분으로 구분한다.
25년 연간 매출은 $1.64B(YoY +28 %)로, 다음과 같이 구성된다.
| 구 분 | 24 매출 ($M) | 25 매출 ($M) | 설 명 |
|---|---|---|---|
| Company‑ operated shops revenue | 1,166 | 1,509 (YoY +29.5%) | 점포 운영 매출 |
| Franchising and other revenue | 115 | 129 (YoY +11.8%) | 로열티, 가맹 지원 등에서 발생하는 매출 |
| Total revenue | 1,281 | 1,638 (YoY +27.9 %) | 154개 신규 출점 |
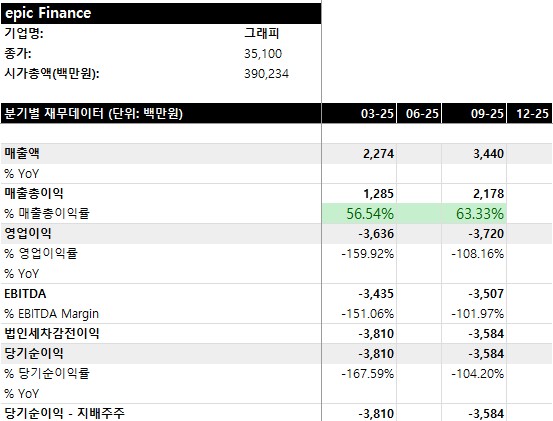
분기별로도 고성장을 이어갔다.
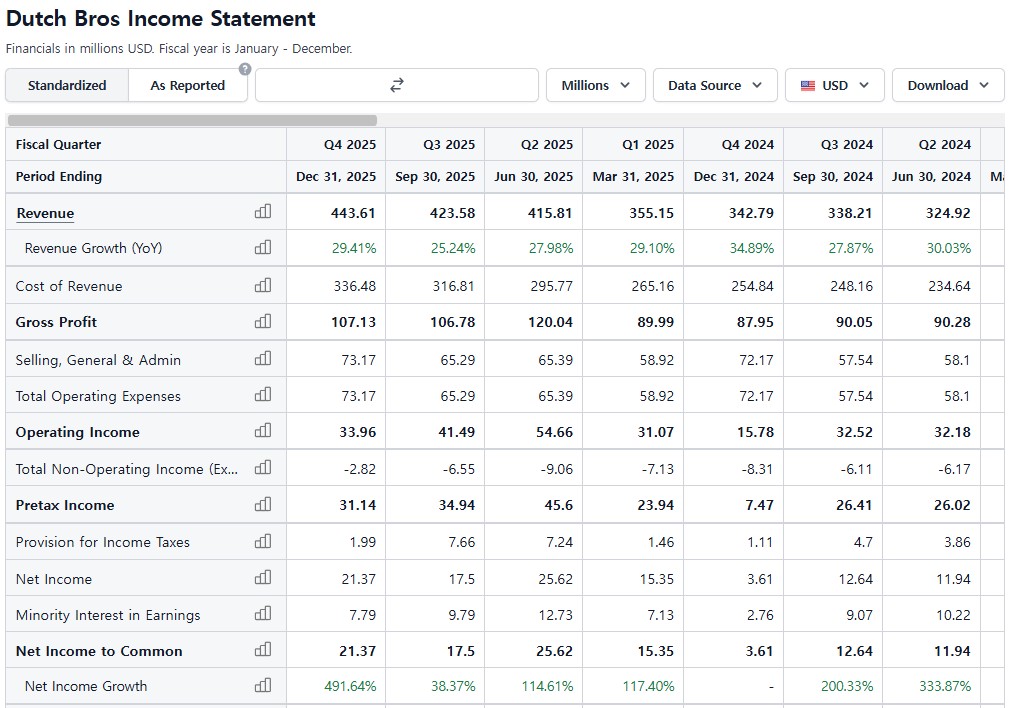
이는 신점포 출점, 기존 점포 매출 증가가 결합된 결과인데, 기여도는 기존 점포 매출 증가가 압도적이라는 점이 인상적이다.
BROS가 소비자들에게 제공하는 가치
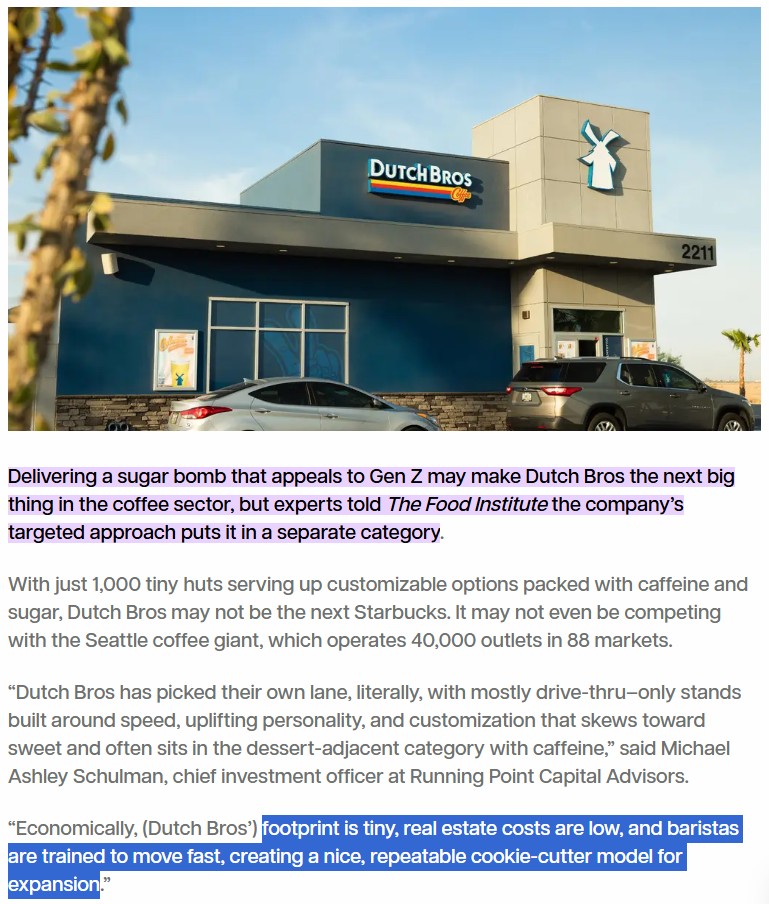
Dutch Bros는 단순히 커피가 아니라 ‘정서적 경험과 편의성’을 판매하는 브랜드다.
감정적 서비스와 커뮤니티 경험
직원(‘Broista’)은 친절한 인사와 대화를 통해 고객에게 위로와 기분 전환을 제공한다.
16년 매장에서 한 직원이 남편을 잃은 여성에게 기도하며 위로하는 사진은 SNS에서 확산되었고, 직원은 이것이 “항상 아픈 사람에게 사랑을 주는 방식”이라고 설명했다.
회사는 경쟁력을 “서비스, 음료 품질, 브로이스타가 제공하는 모든 경험”이라고 강조한다.
그 중에서도 브로이스타가 제공하는 ‘감정적 연결’이 다른 프랜차이즈와 차별화되어 소비자가 재방문하도록 기여하는 무형 자산이다.
빠른 드라이브스루와 작은 점포
Dutch Bros의 매장은 대부분 실내 좌석 없이 드라이브 스루 중심이다.
두 개의 차선을 운영하고 일반적인 드라이브 스루처럼 주문을 수동적으로 기다리기보다 라인 버스터(line‑buster) 직원이 직접 차량으로 가서 주문을 받아 병목을 줄인다.
평균 점포 면적이 약 900 ft²에 불과해 부동산 비용이 낮고, 회전율이 높다.
주문 Ahead (앱 선주문)과 walk‑up 창구도 활용하여 처리량을 높이고 고객 편의성을 강화한다.
맞춤형 음료 플랫폼 : MZ 세대가 선호하는 ‘놀이문화’
Dutch Bros 음료의 90 %가 차가운 음료이며, Rebel 에너지 음료가 매출의 약 25 %이다.
수십 가지 맛과 조합으로 커스터마이즈가 가능해 젊은 소비자층과 SNS에서 인기가 높다.
커피는 매출의 약 절반을 차지해 전통 커피에만 의존하지 않고,
스무디·에너지 드링크·단맛 음료 등으로 고객층을 넓힌다.
데이터 기반 로열티 프로그램
Dutch Rewards 앱은 2025년 말 기준 1,500 만 회원을 보유하고 거래의 72 %가 로열티 프로그램에서 발생했다.
이는 고객 데이터를 축적해 맞춤형 프로모션과 마케팅에 활용하며, 사용자 경험을 주문 Ahead와 결합해 편의성과 재구매를 강화한다.
TAM (Total Addressable Market)
BROS는 25년 Investor Day에서 미국 매장수 목표치(TAM)를 7,000개로 업데이트했다.
이는 브랜드 확장성이 높다는 판단하에 기존 4,000개에서 대폭 상향된 것이다.
내부에서 창출되는 현금흐름으로 29년까지 2,029개 매장을 목표로 성장해나갈 계획이다.
(현재는 서부 위주 25개주에 1,136개 매장을 운영중이다)
목표치는 충분한 실행 전략에 의해 뒷받침되고 있다.
작은 평수의 드라이브스루 매장은 인구 밀도가 높지 않은 교외에서도 출점이 가능하다.
회사는 성장 전략으로 인접 지역(contiguous market) 확장과 자본 효율적(build‑to‑suit) 리스를 강조하며, 평균 점포당 CapEx를 24년 대비 25 % 절감하는 목표를 제시했다.
이는 출점 속도를 유지하면서도 자본 부담을 낮추려는 전략이다.
메가트렌드 – 시장 성장의 논리
소비자 : 편의성 중시와 드라이브스루 문화의 확산
코로나 이후 미국 소비자는 빠르고 비접촉적인 드라이브스루를 선호하는 경향이 강화되었다.
Coffee Intelligence에 따르면, 소비자들은 가격 부담과 신뢰 부족 속에서도 편리함과 개인적 교감을 함께 제공하는 드라이브스루 체인을 선호해 BROS와 같은 브랜드가 성장하고 있다.
Modern Retail은 BROS가 “편의성, 에너지, 아이스”를 바탕으로 26년 181개 신규 출점을 계획중이며, 이는 소비자가 신속함과 에너지 음료를 동시에 원하는 트렌드를 반영한다고 설명했다.
젊은 소비자층 : SNS와 라이프스타일 지향성
Food Institute 기사에 따르면 Dutch Bros는 Z세대와 밀레니얼을 주 타깃으로 하고 있으며,
이들 세대는 포토제닉한 음료, 소셜미디어 공유, 맞춤형 경험을 중시한다.
회사는 드라이브스루 모델로 운영해 임대료를 낮추고 7,000개 매장 체인을 목표로 하고 있다.
이는 젊은 소비자층의 라이프스타일과 도시/교외 주거 패턴을 고려한 전략이다.
음료 시장 변화 : 에너지 음료 시장의 성장
Dutch Bros 매출에서 Rebel 에너지 음료 등 에너지 음료 비중이 25 % 수준이라는 점은 전체 시장 성장과 밀접하다.
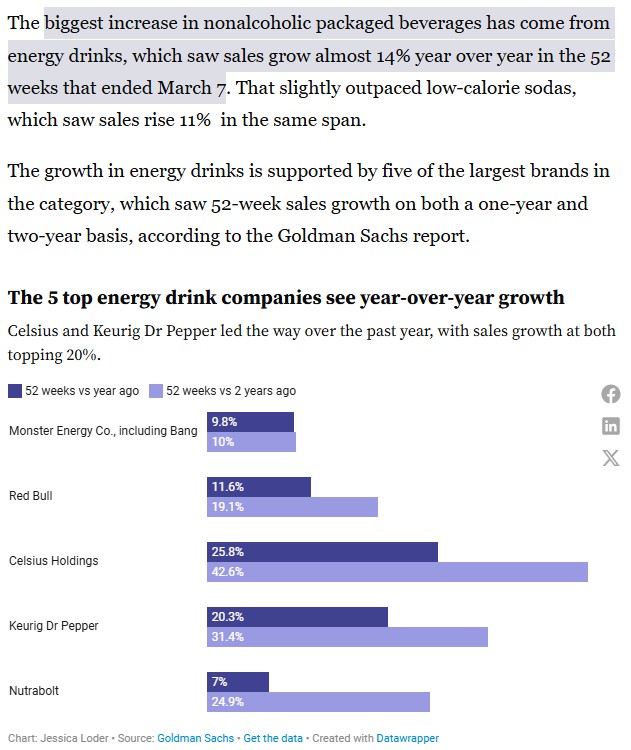
Goldman Sachs는 미국의 에너지 음료 매출은 24년 248억 달러로, 탄산음료에 이어 두 번째로 큰 비알코올 음료 카테고리이며 전년 대비 약 14 % 증가했다고 밝혔다.
다른 음료(탄산, 생수)는 성장률이 1 % 안팎이거나 감소하는 가운데 에너지 음료가 가장 빠르게 성장하는 부문으로 나타났다.
커피 시장 변화 : 카페인 소비 패턴의 변화
Restaurant Dive는 25년 미국의 드립 커피와 콜드브루 주문이 감소한 반면 라떼 주문은 4 %, 에스프레소 샷은 3.3 % 증가했고, 에너지 음료 주문은 8.7 % 증가하며,
카페인 소비 패턴이 다변화되고 있다고 보도했다.
이는 사람들이 기존의 블랙 커피보다 달콤하고 향이 강한 음료나 에너지 드링크를 선호하는 방향으로 이동하고 있음을 의미한다.
BROS의 경제적 해자
무형자산(브랜드·문화)
Dutch Bros의 가장 큰 자산은 사람 중심 문화와 브랜드 이미지다.
고객과 감정적인 연결을 추구하는 브로이스타 문화는 SNS에서 미담이 공유될 정도로 강력하며, 이러한 사람 냄새나는 브랜드 이미지는 일반적인 커피 체인과 차별화된 무형자산이다.
전환비용
전통적인 커피 소비는 브랜드 간 전환이 쉽지만,
Dutch Bros는 로열티 프로그램과 시크릿 레시피를 통해 고객을 묶어두는 장치를 마련했다.
고객은 포인트를 통해 무료 음료를 받거나 선불 충전(Dutch Pass)을 사용해 주문을 간소화한다.
이러한 시스템은 편의성을 높여 재방문을 유도하고, 경쟁사로 이동하려는 유인을 낮춘다.
또한 커스터마이징을 통해 다양한 시크릿 레시피를 개발하고,
이를 SNS에 올리는 ‘놀이문화’를 통해 다른 브랜드에 비해 소비자의 몰입감을 높이고,
더 큰 전환비용을 통해 경제적 해자를 강화할 수 있다.
모방할 수 없는 비용상 우위
Dutch Bros는 작은 점포(약 14~34평)와 드라이브 스루를 통해 임대료를 최소화했다. 10‑K에 따르면 매출의 85 %가 드라이브스루를 통해 발생하며,
매장에는 주차장 대신 차량 대기 차선과 주문창이 배치돼 있다.
따라서 스타벅스 같은 카페형 매장보다 투자 부담이 적고, 출점 속도를 높인다.
또한 매장 규모가 작아 도심 밖 주유소 인근 등 입지 활용도가 높아 경쟁사 대비 확장성이 크다.
이러한 방식의 프랜차이즈 운영은 현재의 선도 사업자들이 매장에서 커피를 소비하는 방식을 추구하고 있어 쉽게 모방할 수 없는 사업 방식으로, 상당 기간 지속되는 우위로 보여진다.
해자와 점유율 전망
해자의 깊이(지속 가능성)
BROS의 브랜드와 문화는 경영진이 강하게 보호하는 핵심 자산이다.
회사는 “사람 우선 문화가 유지되지 않으면 성공이 위험해질 수 있다”고 경고하며 이를 유지하기 위해 리더십 채용과 교육 프로그램에 투자하고 있다.
이런 문화적 차별화는 타 브랜드가 단기간에 모방하기 어렵기 때문에 해자의 깊이는 상당하다.
또한 로열티 프로그램의 높은 침투율과 데이터 기반 개인화는 시간이 지날수록 고도화돼 전환비용을 높일 가능성이 있다.
해자의 넓이(경쟁사의 접근 난이도)
편의성 중심 드라이브스루 모델은 다른 체인도 도입할 수 있지만,
Dutch Bros는 작은 점포, 양방향 차선, 메뉴를 설명하는 브로이스타 등 운영 노하우를 갖고 있어 쉽게 복제하기 어렵다.
그럼에도 차가운 음료와 에너지 드링크 중심 라인업은 경쟁자(스타벅스, 던킨, 편의점, 에너지 음료 회사)가 확장할 수 있는 영역이다.
따라서 해자의 넓이는 중간 수준이며, 경쟁사가 대규모 투자로 모방할 수 있는 여지가 있다.
점유율 전망
Dutch Bros는 커피 체인이지만 실제 경쟁은 에너지 음료, 편의점 음료와 겹친다.
매장수가 25년 1,136개에서 29년 2,029개까지 늘어나면 지역별 접근성이 높아져 점유율이 높아질 것이다.
로열티/감정 서비스가 결합되면 고객 이탈이 감소해 젊은층 중심으로 점유율이 확대될 수 있다.
다만 경쟁사들이 드라이브 스루 혁신과 다양한 차가운 음료를 강화하면 성장이 둔화될 수 있다.
매출 전망
시장 성장성
빠른 음료 수요, 에너지 음료/달콤한 음료 카테고리는 빠르게 증가하고 있다.
에너지, 아이스 음료 시장의 성장 메가트렌드는 BROS 타겟 시장 성장 가능성을 보여준다.
점유율 확대 요소
BROS는 25년 154개, 26년에는 181개 신규 출점을 계획하고 있으며,
이러한 출점 속도는 작은 점포와 낮은 CapEx 덕분에 가능하다.
회사는 에너지 음료와 커스터마이즈 음료 외에도 음식 메뉴와 패키지 음료(CPG)를 확대하고 있어 매출 구성이 다변화될 전망이다.
결국 BROS는 감정적 경험, 자본 효율적인 작은 점포와 빠른 드라이브스루 시스템을 결합해 경쟁사들이 완전히 모방하기 어려운 경제적 해자를 형성했다.
이러한 해자는 문화와 브랜드에 기반한 깊이가 크고, 비용 우위와 운영 효율성 덕분에 매장 확장과 수익성을 동시에 달성하고 있다.
반면 에너지 음료와 맞춤형 차가운 음료 시장은 모방이 가능하기 때문에 경쟁이 치열해질 수 있어 해자의 넓이는 완전하지 않다.
그러나 현재의 메가트렌드(편의성, 달콤한 음료, 에너지 드링크 성장)와 맞물려 Dutch Bros가 상당기간에 걸쳐 매출과 이익을 확대할 가능성이 높다.
BROS의 협상력
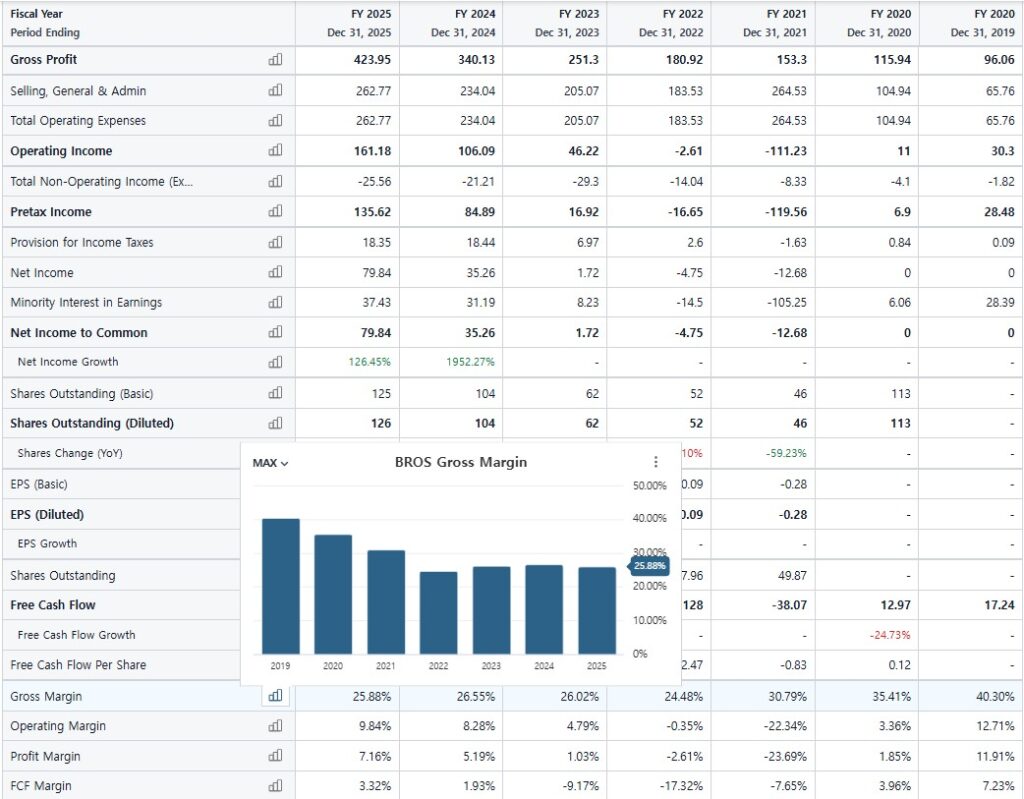
BROS의 GPM은 과거의 40%대에서 20% 중반으로 낮아진 상황이다.
다만, 규모의 경제에 따라 영업이익률과 순이익률이 마이너스에서 높은 한자릿수 수준으로 올라와 있는 상황이다.
회사가 소비자, 시장, 생산요소 제공자 등과 어떤 관계를 맺고 변화시켜나가고 있는지를 바탕으로 이러한 변화의 배경을 확인해보려고 한다.
가격 설정력
25.4Q 컨콜에서 CFO는 고물가 환경에서 가격을 공격적으로 올리기보다 트랜잭션/신규 프로그램(푸드 등)으로 점포당 매출을 늘려나가겠다고 설명했다.
이는 브랜드 충성도가 높아도 가격전가력이 무한하지 않다는 점을 시사한다.
다른 경쟁사, 커피 제품 등과 대체관계가 존재하기 때문에 가격을 과도하게 인상할 경우 소비자를 잃을 가능성이 있다.
비용 통제력
25년 직영점 원가 구조에서 음료·식품·포장(BFP) 비용은 매출의 25.9%로 제시되며,
커피 원가 상승이 마진을 압박했다고 설명한다.
또한 커피 가격 변동의 손익 반영에 2~3분기 시차가 있다고 언급했다.
다만, 커피 가격은 회사가 통제할 수 없기 때문에 헤지/조달/가격-프로모션 조합이 핵심 레버다.
또한, 회사는 build-to-suit(임차인의 요구에 맞춰 건물을 설계, 건설하는 방식) 비중을 늘리며 점포 CapEx를 낮추고 있다고 설명한다(단, 이에 따라 향후 임차 비용 비중이 올라갈 수 있음).
이는 드라이브 스루 BM의 강점을 살려 임차 협상력이 높은 외곽, 접근성이 낮은 지역에 입점하는 전략을 추구한 결과이다.
자본배치와 재무구조
CapEx·FCF·유동성
25.4Q 컨콜에서 “2년 연속 FCF 창출”을 강조했고,
25년 말 점포당 CapEx 하락을 언급했다.
아직 성장기인 사업모델에서 CapEx가 큰데도 FCF가 플러스라는 점에 주목할 필요가 있다.
(가이던스에 따르면 2026 CapEx는 $270~$290M 범위로 증가할 수 있다.)
M&A/전환형 부지 인수 : 개발 효율 관점의 ‘실험’
Clutch Coffee 자산 인수는 10-K에서 “주로 임차권(Right-of-use leases)”을 중심으로 공시됐고, 현금으로 $19.8M을 지불했다.
회사는 2026년 말까지 20개 사이트를 Dutch Bros 직영점으로 전환 개발할 계획이다.
이는 대형 M&A라기보다 입지·개발 속도를 사는 거래에 가깝다.
투자자 관점에서는
1) 전환 후 AUV/마진이 기존 평균을 따라갈지,
2) 향후 유사 딜이 반복될 때 자본효율이 유지되는지,
3) 회사의 문화가 유지되는지
가 체크포인트다.
BROS의 밸류에이션
30% 수준의 매출 성장률, 빠른 수익화, 유기적 성장 위주의 충성도 높은 고객을 감안하면 다소 높은 멀티플은 감수할 수 있다.
다만, 성장 기대가 조금만 충족되지 않아도 멀티플 할인으로 큰 손실을 초래할 위험이 있다.
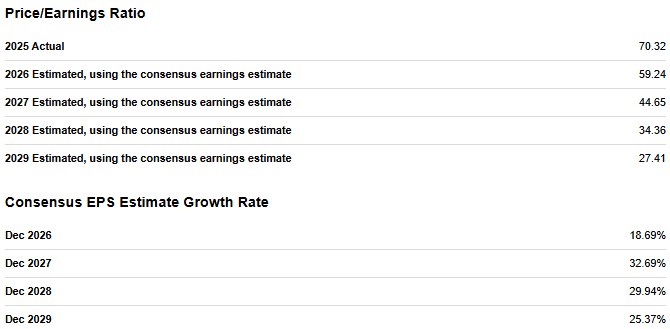
사실 EPS 성장률이 30% 수준을 유지하고, 가이던스를 맞춰간다면 미국 내 유기적 성장만으로도 28~29년 내에 합리적인 수준의 멀티플로 정상화될 수 있는 좋은 BM임은 틀림없다.
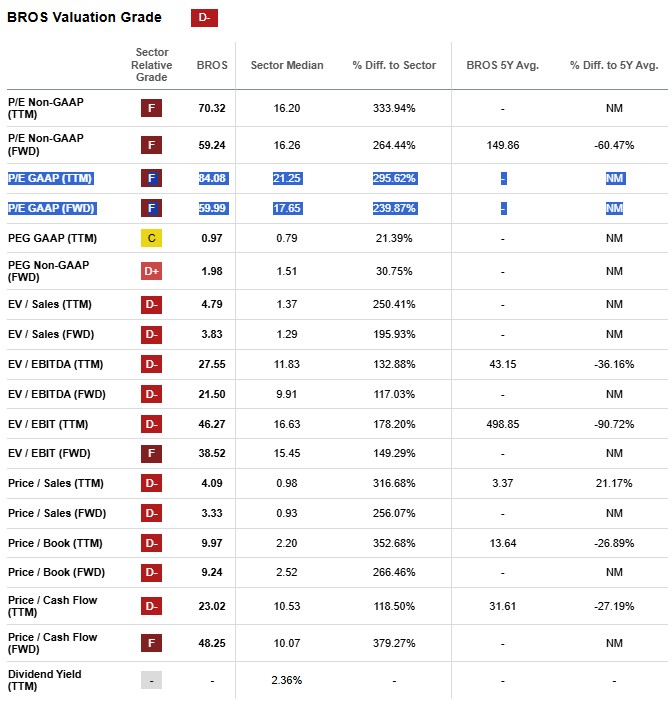
다만, 다수의 프랜차이즈간 경쟁 심화, 성장 과정에서 특유의 문화 이식에의 실패 가능성,
고유의 문화 추구로 인한 성장 지연 가능성, 고용시장 둔화 및 거시경제 리스크로 인한 소득 증가율 둔화 및 지출 감소 가능성 등 수많은 리스크를 고려할 때 현 시총 기준 TTM PER 84.08은 상당한 프리미엄이 포함된 멀티플이라는 생각이 들었다.
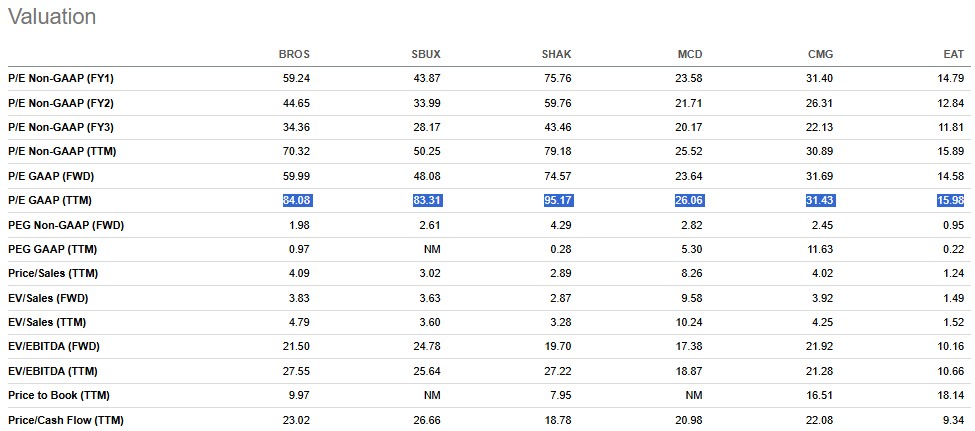
물론 스타벅스, 쉑쉑버거 등 외식 분야 기업 멀티플도 비슷한 수준에서 형성되어 있으나,
그렇다고 성장 둔화로 멀티플이 할인될 BROS 고유의 내재된 위험성이 완화되는 것은 아니다.
(절대적인 멀티플이 높은 수준이다)
BROS가 말하는 성장 내러티브는 실현될 개연성이 충분해 보이며, 계속해서 높은 멀티플을 유지하면서 디지털 시대에 ‘감정 주유소’와 또 하나의 ‘놀이거리로서 음료’를 제공하는 ‘핫플’로서 자리매김할 가능성이 높다고 생각한다.
다만, 치열한 경쟁과 높은 멀티플로 보수적인 관점에서 과도한 비중은 자제하면서, 만약 일시적 노이즈로 안전마진이 확보될 수 있을 정도의 멀티플이 할인된 가격에 거래될 때 커버기업으로 편입해볼 수 있을 것이라고 생각했다.
가치투자 커뮤니티를 성장시켜나가고 있습니다.
운영 계획과 방향성을 한 번 읽어보시고,
텔레그램과 유튜브 채널을 통해 소통하고 있으니 공감이 가신다면 참여해주세요!
쌍방향 소통을 원하는 분들은 카카오톡 채널로 와 주시면 좋을 거 같습니다.
자료실을 통해 리포트, 뉴스도 공유하고 있으니 참고하시면 도움이 될 거 같습니다.